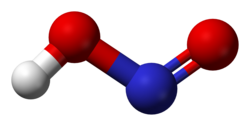
Азотистая кислота
Шаблон:Карточка{{#invoke:check for unknown parameters|check |unknown= |ignoreblank= |preview=Неизвестный параметр «_VALUE_» шаблона Вещество |showblankpositional= |CAS|ChEBI|ChemSpiderID|ECB|EINECS|H-фразы|InChI|InChIKey|NFPA 704|P-фразы|PubChem|R-фразы|RTECS|S-фразы|SMILES|nocat|Кодекс Алиментариус|ЛД50|ООН|ПДК|СГС|большие схемы|вещество1|вещество2|вещество3|вещество4|внешний вид|вращение|гибридизация|давление пара|диапазон прозрачности|динамическая вязкость|дипольный момент|заголовок|изображение|изображение слева|изображение справа|изображение2|изоэлектрическая точка|интервал трансформации|картинка|картинка малая|картинка2|картинка3D|картинка 3D|картинка3D2|кинематическая вязкость|конст. диссоц. кислоты|константа В. дер В.|координационная геометрия|коэфф. электр. сопротив.|кристаллическая структура|критическая плотность|критическая темп.|критическая точка|критическое давление|молярная концентрация|молярная масса|наименование|описание изображений слева и справа|описание изображения|описание изображения слева|описание изображения справа|описание изображения2|описание картинки|описание картинки2|описание картинки3D|описание картинки3D2|описание малой картинки|от. диэлектр. прониц.|плотность|поверхностное натяжение|показатель преломления|предел прочности|пределы взрываемости|примеси|проводимость|растворимость|растворимость1|растворимость2|растворимость3|растворимость4|рац. формула|сигнальное слово|скорость звука|сокращения|состояние|твёрдость|темп. воспламенения|темп. вспышки|темп. кипения|темп. кипения пр.|темп. плавления|темп. разложения|темп. самовоспламенения|темп. стеклования|темп. сублимации|температура размягчения|тепловое расширение|теплопроводность|теплоёмкость|теплоёмкость2|токсичность|традиционные названия|тройная точка|угол Брюстера|уд. электр. сопротивление|удельная теплота парообразования|удельная теплота плавления|фазовые переходы|хим. имя|хим. формула|ширина изображения|ширина изображения2|энергия ионизации|энтальпия кипения|энтальпия образования|энтальпия плавления|энтальпия растворения|энтальпия сгорания|энтальпия сублимации|ЕС|удельная теплота парообразования2|удельная теплота плавления2|Номер UN|эмпирическая формула|теплота парообразования|энтальпия раствородия|тепловое расширодие}}
Азо́тистая кислота́ (химическая формула — HNO2) — слабая одноосновная высокотоксичная неорганическая кислота. При стандартных условиях неустойчива.
Строение
В газовой фазе планарная молекула азотистой кислоты существует в виде двух конфигураций: цис- и транс-.
При комнатной температуре преобладает транс-изомер: эта структура является более устойчивой. Так, для цис-HNO2(г) ΔG°f = −42,59 кДж/моль, а для транс-HNO2(г) ΔG°f = −44,65 кДж/моль.
Физические свойства
Азотистая кислота — это неустойчивая кислота, существующая только в разбавленных водных растворах, окрашенных в слабый голубой цвет, и в газовой фазе. Кислота весьма токсична (в больших концентрациях).
Химические свойства
В водных растворах существует равновесие:
При нагревании раствора азотистая кислота распадается с выделением NO и образованием азотной кислоты:
По действием щелочей образует соли, называемые нитритами (или азотистокислыми), которые гораздо более устойчивы, чем HNO2:
HNO2 является слабой кислотой. В водных растворах диссоциирует (KD = 4,6Шаблон:E), немного сильнее уксусной кислоты:
Используется в органическом синтезе для получения органических нитритов (изопропилнитрита, изоамилнитрита и других). Реакция протекает в присутствии сильных кислот:
Общая реакция:
Азотистая кислота проявляет как окислительные, так и восстановительные свойства. При действии более сильных окислителей (пероксид водорода, хлор, перманганат калия) окисляется в азотную кислоту:
В то же время она способна окислять вещества, обладающие восстановительными свойствами. Реакция с соляной кислотой при незначительном нагревании протекает обратимо, а при температуре выше +100°C идёт необратимо:
Может вступать в реакцию с азидами с образованием более безопасных продуктов, что является способом их утилизации:
Получение
Растворение оксида азота(III) N2O3 в воде:
Растворение оксида азота(IV) NO2 в воде:
Применение
- Диазотирование первичных ароматических аминов и образование солей диазония;
- Применение нитритов в органическом синтезе при производстве органических красителей.
Физиологическое действие
Азотистая кислота (HNOШаблон:Sub) весьма токсична, причём обладает ярко выраженным мутагенным действием, поскольку является дезаминирующим агентом.
ПДК в рабочей зоне 5 мг/м3 (по диоксиду азота).
Источники
- Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. — М.: Химия, 1994.