Этаноламин
Шаблон:Карточка{{#invoke:check for unknown parameters|check |unknown= |ignoreblank= |preview=Неизвестный параметр «_VALUE_» шаблона Вещество |showblankpositional= |CAS|ChEBI|ChemSpiderID|ECB|EINECS|H-фразы|InChI|InChIKey|NFPA 704|P-фразы|PubChem|R-фразы|RTECS|S-фразы|SMILES|nocat|Кодекс Алиментариус|ЛД50|ООН|ПДК|СГС|большие схемы|вещество1|вещество2|вещество3|вещество4|внешний вид|вращение|гибридизация|давление пара|диапазон прозрачности|динамическая вязкость|дипольный момент|заголовок|изображение|изображение слева|изображение справа|изображение2|изоэлектрическая точка|интервал трансформации|картинка|картинка малая|картинка2|картинка3D|картинка 3D|картинка3D2|кинематическая вязкость|конст. диссоц. кислоты|константа В. дер В.|координационная геометрия|коэфф. электр. сопротив.|кристаллическая структура|критическая плотность|критическая темп.|критическая точка|критическое давление|молярная концентрация|молярная масса|наименование|описание изображений слева и справа|описание изображения|описание изображения слева|описание изображения справа|описание изображения2|описание картинки|описание картинки2|описание картинки3D|описание картинки3D2|описание малой картинки|от. диэлектр. прониц.|плотность|поверхностное натяжение|показатель преломления|предел прочности|пределы взрываемости|примеси|проводимость|растворимость|растворимость1|растворимость2|растворимость3|растворимость4|рац. формула|сигнальное слово|скорость звука|сокращения|состояние|твёрдость|темп. воспламенения|темп. вспышки|темп. кипения|темп. кипения пр.|темп. плавления|темп. разложения|темп. самовоспламенения|темп. стеклования|темп. сублимации|температура размягчения|тепловое расширение|теплопроводность|теплоёмкость|теплоёмкость2|токсичность|традиционные названия|тройная точка|угол Брюстера|уд. электр. сопротивление|удельная теплота парообразования|удельная теплота плавления|фазовые переходы|хим. имя|хим. формула|ширина изображения|ширина изображения2|энергия ионизации|энтальпия кипения|энтальпия образования|энтальпия плавления|энтальпия растворения|энтальпия сгорания|энтальпия сублимации|ЕС|удельная теплота парообразования2|удельная теплота плавления2|Номер UN|эмпирическая формула|теплота парообразования|энтальпия раствородия|тепловое расширодие}} Этано̀лами́н HO-CH2CH2-NH2 (глицино́л, 2-аминоэтано́л, тривиальное название коламин) — органическое вещество класса аминоспиртов, является первичным амином и первичным спиртом. Также называется моноэтаноламином для отличия от диэтаноламина (NH(CH2CH2OH)2) и триэтаноламина (N(CH2CH2OH)3).
Физические свойства
Вязкая маслянистая жидкость с температурой кипения 170 °C. Имеет слабый аминный запах. Смешивается с водой во всех отношениях. Хорошо растворим в этаноле, бензоле, хлороформе.
Получение
В промышленности синтез этаноламина проводится присоединением аммиака к этиленоксиду в присутствии небольшого количества воды. Процесс осуществляют в одну стадию при температуре 90—130 °С и давлении 7—10 МПа.
Наряду с моноэтаноламином при этом получаются диэтаноламин и триэтаноламин. При соотношении этиленоксид/аммиак (1:15) в продуктах реакции содержится 78,3 % моно-, 16 % ди- и 4,4 % триэтаноламинов. Этиленоксид в реакции реагирует нацело.
Соотношение этаноламинов в смеси регулируют концентрацией NH3, температурой процесса и повторным направлением в реакцию одного или двух этаноламинов.
Образующуюся смесь этаноламинов, Н2О и NH3 разделяют ректификацией, при этом аммиак в сжиженном виде повторно направляют в реактор.
В лаборатории этаноламин получают действием аммиака на этиленхлоргидрин (2-хлорэтанол):
Химические свойства
Этаноламин — слабое основание (pKa=9.50). С минеральными и сильными органическими кислотами образует соли.
При взаимодействии со сложными эфирами и карбоновыми кислотами или их ангидридами и хлорангидридами моноэтаноламин превращается в соответствующие N-(2-гидрооксиэтил)амиды кислот:
Моноэтаноламин с альдегидами (за исключением формальдегида) и кетонами даёт основания Шиффа, последние обычно находятся в равновесии с изомерными оксазолидинами:

При взаимодействии солей моноэтаноламина с KCN или NaCN и альдегидами и кетонами образуются N-(гидроксиэтил)аминонитрилы:
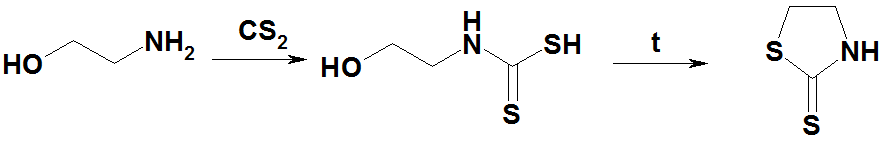
Моноэтаноламин при реакции с CS2 образует N-(2-гидроксиэтил)дитиокарбаминовую кислоту, которая при нагревании даёт меркаптотиазолин:
При нагревании с мочевиной образуется этиленмочевина:

С [[Гамма-бутиролактон|Шаблон:Math-бутиролактоном]] — N-(2-гидроксиэтил)пирролидон, который далее превращается в N-винилпирролидон:

Аммонолиз моноэтаноламина в присутствии Н2 и катализаторов гидрирования (Ni или Cu) приводит к образованию этилендиамину:
Биологическая роль
Этаноламин всегда присутствует в незначительном количестве в организме человека и животных при полноценном белковом питании. В организме он образуется при декарбоксилировании аминокислоты серина. Дальнейшие пути превращений связаны либо с синтезом одного из фосфатидов — кефалина, являющегося фосфатидилэтаноламином, либо с превращением этаноламина в холин.
Применение
Водные растворы этаноламина обладают щелочной реакцией и хорошо поглощают кислые газы (диоксид углерода, диоксид серы, сероводород, а также газообразные и летучие тиолы). При нагреве раствора поглощённые газы выделяются, регенерированный раствор повторно направляют для поглощения. Благодаря обратимости растворы этаноламина широко используются в качестве абсорбента в различных процессах газоочистки (например, удаление примесей сероводорода, углекислого газа и тиолов в нефтегазовой и нефтехимической промышленности) и для разделения газов (в частности, абсорбция углекислого газа из смеси газов при производстве водорода конверсией метана).
Применяется в средствах для окраски волос в качестве заменителя раствора аммиака.
Этаноламин также является исходным веществом в промышленном синтезе таурина.
Безопасность
Моноэтаноламин обладает общетоксическим действием. В соответствии с ГОСТ 12.1.005-76 моноэтаноламин отнесён к токсичным высокоопасным химическим веществам по степени воздействия на организм, 2-го класса опасности[1]. В высоких концентрациях может раздражать кожу и слизистые оболочки. Летальная доза (ЛД50 100-149 мг/кг[2] (для белых мышей, перорально).
При остром отравлении возникает раздражение слизистых оболочек, урежение дыхания, двигательное возбуждение, судороги. У белых крыс, вдыхавших воздух с концентрацией моноэтаноламина 0,2—0,4 мг/л по 5 часов ежедневно в течение 6 месяцев наблюдались изменения функционального состояния центральной нервной системы и функций печени, незначительная анемия и ретикулоцитоз, повышенный диурез и белок в моче.
Крысы, подвергавшиеся практически непрерывному отравлению в течение 30 суток при концентрации 0,164 мг/л, погибали через 14—24 суток, но выживали в тех же условиях в течение 90 дней при концентрации 0,029 мг/л. Морские свинки при непрерывном вдыхании 0,184 мг/л погибали между 10 и 28 днём. Концентрация 0,037 мг/л переносилась в течение 90 суток, а 0,12 мг/л вызывала лишь слабые признаки отравления. Собаки пережили в течение 30 дней вдыхание 0,25 мг/л и 0,015 мг/л в течение 60 дней[3].
Санитарная норма по ПДК в воздухе рабочей зоны - 1 мг/м3 (рекомендуемая)[4].
Примечания
Литература
- ↑ ГОСТ 12.1.005-76 Система стандартов безопасности труда (ССБТ). Общие санитарно-гигиенические требования к воздуху рабочей зоны
- ↑ ГОСТ 12.1.007-76 Система стандартов безопасности труда (ССБТ). Вредные вещества. Классификация и общие требования безопасности
- ↑ Шаблон:Публикация
- ↑ ГОСТ 12.1.005-88. Система стандартов безопасности труда (ССБТ). Общие санитарно-гигиенические требования к воздуху рабочей зоны (с Изменением N 1)